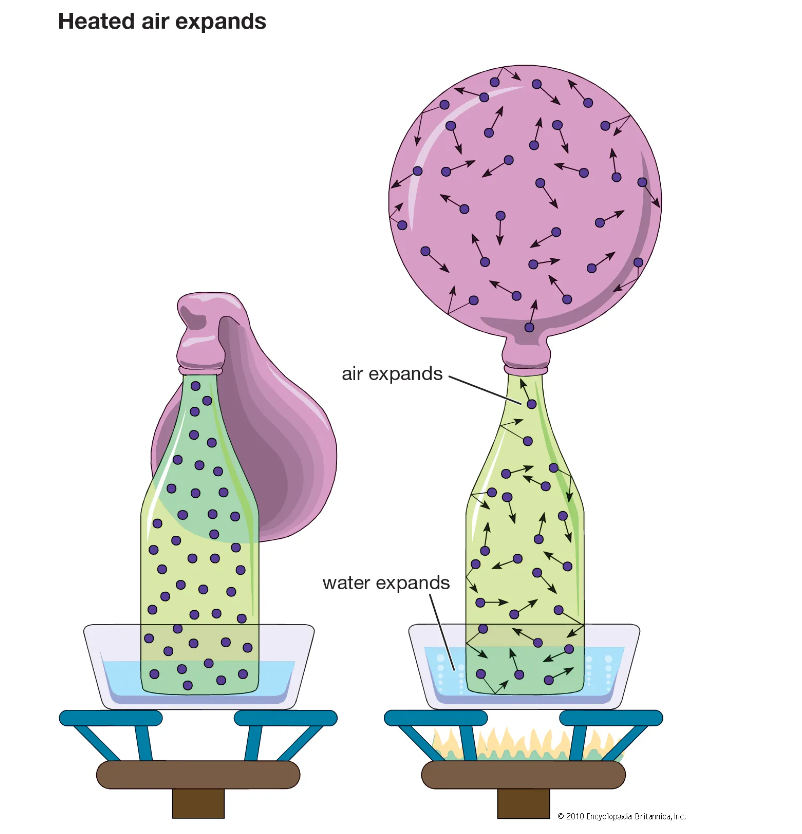
Gaz , Maddenin belirli bir şekli olmayan, çok akışkan olduğu ve sıvıların yoğunluğunun yaklaşık %0,1'i kadar yoğunluğa sahip olduğu maddenin üç temel halinden biridir. Gaz çok sıkıştırılabilir ama süresiz olarak genişleme eğilimindedir ve herhangi bir kabı doldurur. Sıcaklık veya basınçtaki küçük bir değişiklik, hacminde önemli bir değişiklik yaratır; bu ilişkiler gaz yasalarında denklemler olarak ifade edilir. 19. yüzyılda geliştirilen gazların kinetik teorisi, gazları sürekli hareket halindeki küçük parçacıkların (atomlar veya moleküller) toplulukları olarak tanımlar ve davranışlarının anlaşılmasına büyük katkıda bulunur. Gaz terimi aynı zamanda benzin, doğal gaz veya anestetik nitröz oksit anlamına da gelebilir.
Sıvı ve katı hallerden belirgin şekilde farklı özelliklere sahip, maddenin üç temel halinden biri olan gaz . Gazların dikkat çekici özelliği, hiçbir yapıya sahip değilmiş gibi görünmeleridir. Ne belirli bir büyüklükleri ne de şekilleri vardır, halbuki sıradan katıların hem belirli bir boyutu hem de belirli bir şekli vardır ve sıvılar, şekillerini içine konulduğu kabınkine uydursalar bile, belirli bir boyuta veya hacme sahiptirler.
Seyreltik bir gazın küçük bir hacmindeki muazzam sayıdaki moleküller, beklenebileceği gibi karmaşıklık değil, basitleştirme üretir. Bunun nedeni, gazların davranış ve özelliklerinin incelenmesinde genellikle yalnızca istatistiksel ortalamaların gözlemlenmesi ve büyük sayılar söz konusu olduğunda istatistiksel yöntemlerin oldukça doğru olmasıdır. İlgili moleküllerin sayısıyla karşılaştırıldığında, burada dikkat edilmesi gereken gazların yalnızca birkaç özelliği vardır: basınç, yoğunluk, sıcaklık, iç enerji, viskozite, ısı iletkenliği ve yayılma.